Почвенные минералы и питание
растений
Авторы: Balwant Singh, (Департамент наук об
окружающей среде Сиднейского университета) и Darrell G. Schulze (Кафедра агрономии Университета
Пердью) © 2015 Nature
Education
Ccылка: Singh, B. и Schulze, D. G.
(2015) Почвенные минералы и питание растений. Знание о природе 6 (1): 1
Как
химические реакции с участием почвенных минералов играют решающую роль в
контроле доступности основных питательных веществ для растений?

Всем растениям требуется
17 элементов для завершения их жизненного цикла, а еще четыре элемента были
определены как необходимые для некоторых растений (Havlin et al. 2005). За
исключением C, H и O, которые растения получают из воздуха и воды, остальные 14
элементов растения получают из почвы или с помощью
удобрений, навоза и добавок (Parikh и James 2012).Основную часть твердой
фракции почвы составляют почвенные минералы, которые оказывают значительное
прямое и косвенное влияние на снабжение и доступность большинства питательных
элементов. К основным процессам выделения и фиксации элементов питания в почвах
относятся растворение-осаждение и адсорбция-десорбция. Мы обсудим эти процессы
и то, как они влияют на макроэлементы и микроэлементы.
Первичные минералы и
плодородие почвы
Осадочные
породы покрывают 75-80% земной коры и образуют исходные (материнские) материалы
для подавляющего большинства почв. Исходный (материнский) материал почвы
оказывает значительное прямое влияние на содержание питательных элементов в
почве; это влияние более выражено в молодых почвах и несколько уменьшается с
увеличением возраста почвы и ее выветривания. Чтобы лучше понять влияние
исходных (материнских) материалов почвы (почвообразующих пород) на элементный
состав почвы, полезно рассмотреть минералогический состав обычных горных пород,
слагающих исходный (материнский) материал почвы
(почвообразующую породу) (табл. 1). Первичные минералы образуются при
повышенных температурах из остывающей магмы во время первоначального
затвердевания породы или во время метаморфизма, и они обычно происходят из
магматических и метаморфических пород в почве (Lapidus, 1987). В большинстве
почв основными первичными минеральными составляющими являются полевые шпаты,
слюды и кварц, в меньших количествах присутствуют пироксены и роговые обманки.
|
Минералогический состав |
Вулканические породы |
Сланцы |
Песчаники |
Состав (содержание) микроэлементов |
|
|
% |
Базовый |
Мобильный (не всегда) |
|||
|
Полевые шпаты |
59.5 |
30.0 |
11.5 |
K,
Ca, Na |
Cu,
Mn |
|
Амфибол и пироксен |
16.8 |
– |
sm |
Mg,
Fe, Ca |
Ni,
Co, Cu, Mn, Zn, Mo |
|
Слюда |
3.8 |
– |
sm |
K,
Ca, Na, Mg, Fe |
Ni,
Mn, Co, Zn, Cu |
|
Минералы титана |
1.5 |
– |
sm |
Ti,
Fe, Ca |
Co,
Ni |
|
Апатит |
0.6 |
– |
sm |
Ca,
P |
|
|
Глина |
– |
25.0 |
6.6 |
K,
Mg, Fe, Ca, Na |
|
|
Оксиды железа |
– |
5.6 |
1.8 |
Fe |
Mn,
Zn, Ni, Co |
|
Карбонаты |
– |
5.7 |
11.1 |
Ca,
Mg, Fe |
|
|
Прочие полезные ископаемые |
– |
11.4 |
2.2 |
– |
– |
Таблица 1: Средний минералогический и элементный состав обычных горных пород на Земле (по данным F.W. Clarke, Klein and Hurlbut, 1999). |
|||||
Первичные минералы, в
том числе калиевые полевые шпаты (ортоклаз, санидин и микроклин), слюды
(мусковит, биотит и флогопит) и глинистые слюды (иллит), широко распространены
в большинстве типов почв, за исключением сильно выветреных и песчаных почв. Эти
первичные минералы действуют как важный резервуар для калия, при этом более 90%
калия в почвах существует в структуре этих минералов. В полевых шпатах также
присутствуют значительные количества Ca, Na и Si и меньшие количества Cu и Mn.
Слюды и иллит являются наиболее важными источниками калия во многих почвах, а
также содержат Mg, Fe, Ca, Na, Si и ряд питательных микроэлементов. Амфиболы и
пироксены являются жизненно важными резервуарами Mg, Fe, Ca, Si и большинства
микроэлементов. Карбонатные минералы, в том числе образованные из исходного
(материнского) материала почвы и образующиеся в почве в результате педогенных
процессов, служат как источником, так и поглотителем Ca и Mg в почвах.
Физическое, химическое и
биологическое выветривание первичных минералов высвобождает ряд питательных элементов в
почвенный раствор. Скорость выветривания и пути первичных минералов сильно
различаются и зависят от нескольких факторов, включая свойства минералов и
климатические условия. Хотя скорости выветривания
первичных минералов для определенных элементов могут быть недостаточно высокими
для удовлетворения потребностей растений в питательных веществах на
краткосрочной основе, особенно в системах управляемого земледелия, выветривание
минералов является важным и долгосрочным источником нескольких питательных
веществ, полученных геохимическим путем.
Вторичные минералы и
плодородие почвы
В отличие от первичных
минералов вторичные минералы в почвах обычно образуются в результате
низкотемпературных реакций при выветривании первичных минералов в водной среде
на поверхности Земли. Вторичные минералы в первую очередь контролируют
питательные вещества посредством реакций адсорбции-десорбции,
растворения-осаждения и окислительно-восстановительных реакций. Реакции
адсорбции с участием минералов часто более важны для контроля доступности
питательных элементов для растений, чем высвобождение питательных элементов в
результате выветривания минералов. Филлосиликаты с постоянным зарядом
(например, вермикулит и смектит) предлагают места обмена, которые содержат ряд
необходимых питательных веществ в их катионной форме (емкость катионного
обмена), таких как Ca2+, Mg2+, K+ и Na+; питательные
вещества сохраняются за счет образования внешнесферных комплексов (рис. 1) и
могут легко поглощаться корнями растений. С
другой стороны, минералы с переменным зарядом (например, оксиды железа)
сохраняют некоторые питательные вещества (P, Zn), образуя внутрисферные
комплексы (рис. 2), и такие питательные вещества нелегко доступны для растений.
Важные реакции, относящиеся к конкретным питательным элементам, обсуждаются
ниже.
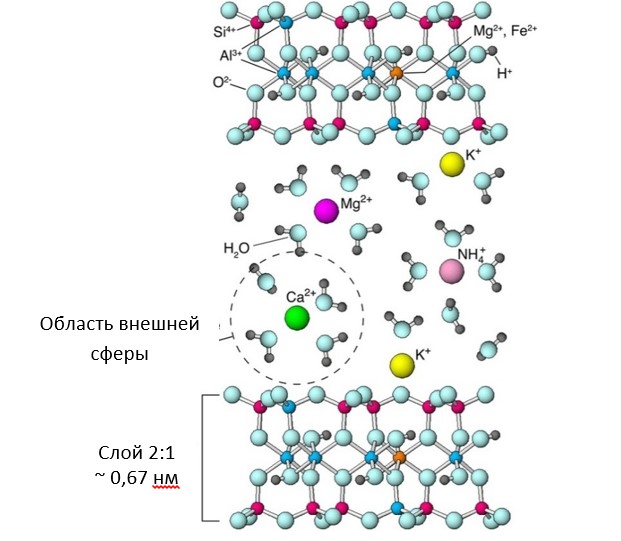
Рисунок 1: Гидратированные
обменные катионы в межслоевой области глинистого минерала смектита.
©
2014 Nature Education Предоставлено Balwant Singh и Darrell G. Schulze. Все
права защищены.
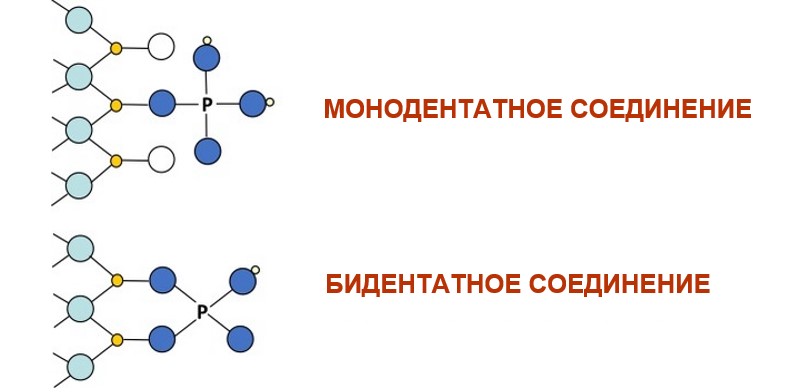
Рисунок 2: Схематическое
представление адсорбции фосфатов путем образования комплексов внутренней сферы
с участием монодентатных и бидентатных связей на поверхности гетита.
© 2014 Nature Education Предоставлено Balwant Singh и Darrell G. Schulze
Все права защищены.
Азот: растения обычно поглощают нитратную (NO3-) и аммонийную (NH4+) формы почвенного азота. В почвах азот, внесенный в виде удобрений, и минерализованный азот из органического вещества в основном переходят в форму NO3-. Из-за ограниченной емкости анионного обмена большинства почв выщелачивание внесенного азота в виде ионов NO3- является распространенной проблемой качества воды, особенно в сельскохозяйственных регионах. Это также представляет собой важную экономическую неэффективность, поскольку производители применяют чрезмерное количество удобрений, чтобы компенсировать выщелачивание. Исключением являются сильно выветренные почвы, такие как оксисоли и ультисоли (oxisols and ultisols). В минералогическом составе оксисолей и ультисолей (oxisols and ultisols) преобладают минералы с переменным поверхностным зарядом, в основном каолинит и оксиды железа и алюминия, которые придают этим почвам способность удерживать большие количества NO3-N, особенно в подпочвенных горизонтах. Например, Lehmann и др. (2004) наблюдали 150–300 кг NO3-N на га-1 (на глубину до 2 м) в бразильской оксисоли (oxisol) в системе выращивания кукурузы и сои. Кроме того, Rasiah и Armor (2001) оценили от 17 000 до 32 000 кг NO3-N на гектар на глубину 10 м при различных видах землепользования в оксисолях (oxisols) северного Квинсленда в Австралии. Ёмкость анионного обмена австралийских оксисолей (oxisols) была высокой и достигала 41 mmolc kg-1. Адсорбированный нитрат находится слишком глубоко и, вероятно, недоступен большинству полевых культур, тем не менее, он не вымывается в грунтовые воды.
В отличие от сильно
выветреных оксисолей и ультисолей (oxisols and
ultisols) с минералами переменного заряда, почвы в регионах с умеренным
климатом обычно имеют минералы с постоянным зарядом (например, смектит и
вермикулит) с высокой ёмкостью катионного обмена и способностью удерживать ионы
аммония (NH4+). Действительно, большая часть NH4-N
сохраняется в промежуточных слоях филлосиликатов 2:1 и не поддается легкому
обмену, поэтому его называют фиксированным NH4. Процесс NH4-фиксации
аналогичен K-фиксации, что показано на рис. 3. В фиксации ионов NH4+
в почвах участвуют вермикулит, иллит и межслоистые минералы с соотношением
слоев 2:1. За исключением песчаных почв, количество связанного NH4+
в почве колеблется от 350 до 3 800 кг NH4-N
на га-1 в верхних 30 см почвы; вермикулит и частично выветреный иллит обычно
обладают большей способностью фиксировать NH4+ в почвах,
чем смектитовая группа минералов (Nieder и друг. 2011; Nörmik и Vahtras 1982;
Stevenson и Cole 1999). Различное поведение и способность филлосиликатов 2:1
связывать ионы NH4+ связаны с величиной и происхождением
отрицательного заряда в этих минералах. Фиксация NH4 обычно
увеличивается с увеличением заряда слоя в филлосиликатах 2:1, и фиксация больше
в минералах с зарядом, возникающим в тетраэдрическом слое, чем в минералах с
зарядом, возникающим в октаэдрическом слое.
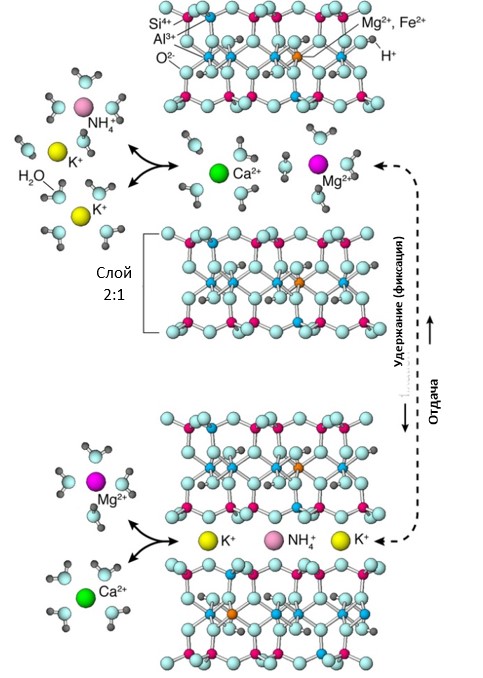
Рисунок 3: Фиксация K+ и NH4+
происходит, когда эти одновалентные катионы из почвенного раствора (вверху
слева) вытесняют гидратированные катионы (показаны как Ca2+ и Mg2+)
из промежуточного слоя вермикулита (вверху справа). Катионы K+ и/или NH4+
дегидратируются и плотно удерживаются в полостях противоположных слоев 2:1,
образуя структуру, аналогичную слюде (внизу справа), в то время как вытесненные
катионы перемещаются в почвенный раствор (внизу слева). Обратная реакция
приводит к высвобождению фиксированных катионов.
©
2014 Nature Education Предоставлено Balwant Singh и Darrell G. Schulze. Все
права защищены.
Фосфор:
P в основном поглощается растениями в форме ионов фосфата (HPO42- и
HPO4-) из почвенного раствора. Концентрация фосфора в почвенной
воде, как правило, очень низкая (<0,01% от общего содержания фосфора в
почве), при этом основная часть почвенного фосфора существует в виде
органического фосфора, нерастворимых соединений фосфора с алюминием, железом и
кальцием, а также фосфатов, адсорбированных на оксиды и филлосиликаты Fe и Al
(Stevenson и Cole 1999; Brady и Weil 2008). Ионы
фосфатов из растворенных химических удобрений быстро реагируют в большинстве
почв, что приводит к фиксации
фосфора в почве. Эти почвенные реакции включают процессы как адсорбции, так и
осаждения.
(i) Реакции адсорбции
Реакции
адсорбции ионов фосфатов на минеральных поверхностях преимущественно связаны с
образованием внутрисферных комплексов на поверхностях с переменным зарядом
оксидов Fe и Al и каолинитов. Пример
представлен на рисунке 2, где ионы фосфата адсорбируются на поверхности гетита,
образуя монодентатные и бидентатные связи. Ионы фосфатов, адсорбированные
такими процессами, лишь медленно становятся доступными для растений. Также
известно, что фосфат сорбируется кальцитом в известковых почвах, при этом
сорбция происходит за счет замещения CO32- на поверхности
кальцита.
(ii) Реакции осаждения
В
сильнокислых почвах реакции осаждения с участием растворимого фосфата из
удобрения приводят к образованию нерастворимых фосфатов Al, Fe или Mn. Напротив,
в известковых почвах образуются нерастворимые фосфаты кальция, которые
постепенно превращаются в нерастворимый карбонатный гидроксиапатит. Общие
химические реакции фосфатов в кислых и известковых почвах
представлены ниже:

Калий:
среди основных элементов калий обычно наиболее распространен в почвах. Общее
количество калия в почвах колеблется от 0,5 до 2,5% от массы почвы, и большая
часть калия существует в минеральной форме (калиевые полевые шпаты и слюды).
Калий высвобождается в результате выветривания или растворения минералов калия
в почве, как показано в следующих примерах:

Из этих двух реакций
высвобождение калия при выветривании слюды, как правило, более важно для
снабжения растений калием в неудобренных почвах.
Филлосиликаты
сохраняют и выделяют для растений К из необменных или фиксированных (т.е. обмениваемых
очень медленно и только тогда, когда концентрация К в почвенной воде падает
ниже порогового значения) и обменных форм. Ионы калия, присутствующие на
участках обмена, поглощаются за счет комплексообразования внешней сферы и легко
доступны для поглощения растениями (рис.
1). С другой стороны, иллит, вермикулит и межслоистые глинистые минералы 2:1
высвобождают фиксированный или необменный калий из межслоевых участков
посредством процессов катионного обмена и диффузии с более низкой скоростью, чем
обменный калий (рис. 3). Подобно ионам NH4+, калий, поступающий с
удобрениями или другими добавками, может фиксироваться в прослойках минералов
2:1 (рис. 3). Необменный или фиксированный калий потенциально может вернуться
обратно в почвенный раствор, если концентрация калия в растворе упадет ниже
определенного порогового значения.
Вторичные питательные вещества
Среди вторичных
питательных веществ Ca и Mg поглощаются растениями в их катионных формах, Ca2+
и Mg2+. Эти катионы удерживаются на отрицательно заряженных участках
филлосиликатов за счет электростатического притяжения (комплексообразование
внешней сферы) (рис. 1). Осаждение вторичных карбонатов, таких как кальцит
(CaCO3), кальцит магния (Ca1-xMgxCO3) и гипс (CaSO4.2H2O),
является обычным явлением в почвах засушливых и полузасушливых сред. Вторичные
карбонаты считаются важными поглотителями некоторых питательных веществ за счет
включения в структуру минерала (например, Mn) или комплексообразования внутри
сферы (например, P и Zn) на поверхности минерала. Сера поглощается растениями в
виде сульфата (SO42-), и это наиболее распространенная
неорганическая форма серы в почвах. Оксиды Fe и Al, а также каолинит являются
местами адсорбции SO42- в большинстве почв, даже если эти минералы
присутствуют в небольших количествах. Считается, что сульфат-ионы поглощаются
этими минералами, образуя как внутри -, так и внешнесферные комплексы. В
известковых почвах SO42- может сорбироваться на CaCO3,
образуя соосаждение CaCO3-CaSO4, что делает SO42-
недоступным для растений. Сульфидные (S-, S2-) минералы образуются в
восстановительных средах (например, в пресноводных и приливных болотах), где
ионы SO42- восстанавливаются с образованием таких минералов, как
пирит (FeS2). Такие восстановленные формы S окисляются на воздухе,
высвобождая ионы SO42-, H+ и Fe3+ в почвенный раствор.
Микроэлементы
(питательные вещества)
Среди микроэлементов Fe, Mn,
Cu, Zn и Ni поглощаются растениями в их катионных формах, а B, Mo и Cl — в
анионных формах. Fe и Mn часто присутствуют в больших количествах в большинстве
почв, и реакции адсорбции играют небольшую роль в контроле их доступности для
растений в почвах. Реакции окисления и осаждения преимущественно контролируют
концентрацию Fe и Mn в почвенном растворе. Гетит, гематит и ферригидрит
являются наиболее часто встречающимися в почвах вторичными оксидами железа.
Из-за микрокристаллического размера оксидов железа эти минералы обладают
высокой удельной (характерной) поверхностью и обеспечивают многочисленные места
адсорбции как катионных, так и анионных элементов во всех разновидностях почв.
Известно,
что два наиболее устойчивых оксида Fe, гетит и гематит, имеют существенное
структурное замещение микроэлементов, включая Mn, Ni, Zn и Cu. Минералы
марганца не так многочисленны и распространены, как оксиды Fe. Часто они
существуют в почвах в виде минеральных покрытий, конкреций (узелков) или
тонкодисперсных частиц в почвенной матрице. Оксиды Fe и Mn являются обычными
минеральными составляющими во многих почвах и важными субстратами для удержания
многих макроэлементов и микроэлементов. Доступность для растений как Fe, так и
Mn значительно снижается в известковых почвах из-за чрезвычайно низкой
растворимости оксидов Fe и Mn и карбонатов Mn. В таких ситуациях растения
вызывают биохимические реакции, такие как высвобождение восстанавливающих и
хелатирующих соединений и подкисление ризосферы, что может увеличить
доступность Fe, Mn и других питательных микроэлементов.
Медь, Zn и Ni
адсорбируются оксидами Fe и Al, образуя внутрисферные комплексы при низких
концентрациях растворов. Однако при более высоких концентрациях раствора
происходит осаждение гидроксидов металлов (Ginder-Vogel и Sparks 2010). Адсорбция Cu2+, Zn2+ и
Ni2+ происходит за счет образования внешнесферных комплексов на
отрицательно заряженных поверхностях филлосиликатов 2:1 и, возможно, за счет
образования внутренних комплексов на поверхностях каолинитов. В щелочных почвах
также может происходить адсорбция Zn на кальците и соосаждение Cu в кальците. B
и Mo поглощаются растениями в виде H3BO3 и MoO42-.
Ограниченные данные свидетельствуют о том, что виды B (т.е. B(OH)3 и
B(OH)4-) в почве адсорбируются путем образования внутрисферных
комплексов на поверхности оксидов Fe и Al (Su & Suarez 1995). Точно так же
MoO42- сильно адсорбируется оксидами металлов. Хлор поглощается
растениями в хлоридной (Cl-) форме, и реакции адсорбции с участием ионов Cl
аналогичны реакциям с участием ионов NO3-. Следовательно,
относительно высокий потенциал обменной адсорбции ионов Cl возникает в сильно
выветреных почвах, поскольку в их минералогии преобладают минералы с переменным
зарядом, такие как каолинит и оксиды Fe и Al. В некоторых почвенных средах,
таких как почвы с ограниченным выщелачиванием или в низкорасположенных районах
с засушливым климатом, Cl может существовать в виде осажденных минеральных
форм, таких как NaCl, CaCl2 и MgCl2.
Заключение
Почвенные минералы служат как
источниками, так и поглотителями основных питательных веществ растений.
Поскольку первичные минералы, первоначально образовавшиеся при высоких
температурах и давлениях в изверженных и метаморфических породах, выветриваются
в почвах, они высвобождают питательные вещества растений в почвенный раствор.
Новые минералы образуются в водной фазе почвенных сред. Эти вторичные минералы
сами служат источниками питательных веществ, либо они осаждают или адсорбируют
необходимые элементы, препятствуя их поглощению растениями.
Во
многих случаях вторичные минералы служат важными резервуарами, в которых
питательные вещества удерживаются достаточно сильно, чтобы предотвратить
выщелачивание, и в то же время достаточно слабо, чтобы растения могли
использовать их для удовлетворения своих потребностей в питании.В некоторых
почвах и в некоторых верхних слоях почвы органическая материя (вещество) почвы
содержит и выделяет питательные элементы для растений.